- Методы
- Общие сведения
- Определение, цели, показатели нормы
- Зачем измерять значение ПСА?
- Сопутствующие диагностические методы
- Лабораторные симптомы рецидива рака простаты
- Системный рецидив после радикальной простатэктомии
- Местный рецидив после простатэктомии
- Диагностика и лечение рецидива рака простаты
- Рецидив рака простаты — лечение в Москве
- PSA после лечения онкологии
- ПСА после простатэктомии
- Как часто нужно сдавать кровь на анализ?
- ПСА после лучевого воздействия
- Как часто нужно делать анализ?
- Лечение рецидивов
- Биохимический рецидив после радикальной простатэктомии
- Лечение рецидива рака и PSA-тест
Методы
Выполнен систематически обзор с включением клинических исследований (в них входили не менее 100 пациентов), найденных в базах данных Medline, Medline In-Process, Embase и Cochrane Central Register of Controlled Trials.
Увы, но даже в случае успешно проведенного радикального лечения болезнь может вернуться. Чтобы своевременно выявить рецидив, необходимо регулярно сдавать анализ крови на ПСА после операции рака простаты: норма данного онкомаркера, факторы, влияющие на отклонение от нее, а также правильная подготовка к исследованию — об этих и некоторых других важных аспектах ПСА-теста мы расскажем ниже.
Вероятность рецидива злокачественной опухоли предстательной железы в первые 10—12 лет после операции составляет от 30 до 50%.
Общие сведения
Рецидив рака простаты – злокачественное новообразование, возникшее через несколько месяцев либо лет после радикального консервативного или оперативного лечения рака предстательной железы. Может быть местным (развившимся в облученной ткани простаты либо в области ложа удаленной предстательной железы), системным (сопровождающимся метастатическим поражением отдаленных органов) либо биохимическим (проявляющимся только в виде увеличения уровня ПСА). В течение 10 лет после завершения терапии локальные и системные рецидивы рака простаты выявляются у 27-53% больных. Данные о распространенности биохимических рецидивов разнятся. Лечение проводят онкологи, урологи и андрологи.

Определение, цели, показатели нормы
ПСА (PSA), или простатспецифический антиген — это фермент, который продуцируется исключительно предстательной железой. В крови здорового мужчины его количество минимально. Превышение нормы ПСА может свидетельствовать о наличие в организме патологических процессов.
Зачем измерять значение ПСА?
В зависимости от возраста пациента коэффициент нормы простатспецифического антигена отличается.
Норма ПСА после удаления рака простаты в определенных случаях не совпадает с вышеназванными показателями. Разберем этот вопрос подробнее в следующей части статьи.
29 октября 2020
Даже после тщательно проведённой операции по поводу злокачественной опухоли простаты есть риск возврата болезни. Раковые клетки могут остаться в сопредельных с железой тканях, шейке мочевого пузыря, прямой кишке. Последующая лучевая или химиотерапия не всегда даёт эффект. Причиной неэффективности лечения рака простаты часто оказывается позднее обращение за помощью.
При I–II стадии рака и своевременном лечении возможно полное излечение, когда аденокарцинома достигла III–IV степени, высок риск рецидива.
Степень риска зависит:
После лапароскопической радикальной простатэктомии удалённые ткани отправляют на гистологическое исследование. Результаты оценивают по шкале Глисона: чем больше найдено мутировавших, низкодифференцированных клеток, тем хуже прогноз.
Рецидив бывает биохимическим, местным и системным.

Важный маркер возвращения опухоли — повышение в крови ПСА.
Сопутствующие диагностические методы
При подозрении на повторное возникновение онкологии недостаточно провести одно исследование — для точной диагностики заболевания врач может назначить следующие мероприятия.
Чтобы результаты анализа были максимально точны, необходимо соблюдать несложные рекомендации:

Повышение ПСА в крови после удаления простаты или облучения не всегда свидетельствует о повторном заболевании. Чтобы поставить точный диагноз, необходимо провести анализ несколько раз, а в спорных случаях пройти дополнительное обследование, которое подтвердит или опровергнет биохимический рецидив рака простаты.
Лабораторные симптомы рецидива рака простаты
В 1999 году было установлено, что рецидив злокачественной опухоли простаты обязательно сопровождается увеличением уровня ПСА (простатического специфического антигена). Это открытие изменило подход к диагностике заболевания и обусловило увеличение роли лабораторных исследований в процессе выявления рецидивов рака предстательной железы. Появилось новое понятие – биохимический рецидив рака простаты (ПСА-рецидив). Широкое внедрение лабораторных методов диагностики данной патологии позволило обеспечить раннюю диагностику рецидивных процессов и увеличить долю радикальных методов лечения.
Увеличение уровня ПСА может быть обусловлено как развитием рецидива рака простаты, так и наличием оставшихся нормальных клеток предстательной железы в области ложа удаленного органа. Дифференциальную диагностику локальных рецидивов рака простаты, системных процессов и увеличения уровня ПСА, обусловленного оставшимися клетками предстательной железы, осуществляют с учетом исходного уровня простатического специфического антигена, скорости его прироста и времени удвоения.
Установлено, что спустя 5 лет с момента выявления биохимического рецидива летальный исход наступает у 4%, спустя 15 лет – у 15% пациентов с биохимическим рецидивом рака простаты. Всего 15% больных погибает от прогрессирования заболевания, при этом средняя продолжительность периода между повышением уровня ПСА и наступлением смерти составляет 13 или более лет. Данная статистика указывает на существование подгруппы повышенного риска внутри группы пациентов с диагностированным биохимическим рецидивом рака простаты, однако определение критериев отбора лиц, входящих в эту подгруппу, пока представляет собой серьезную проблему.
— После удаления предстательной железы уровень антигена в крови не упал до нуля. Означает ли это, что выбранный метод лечения неэффективен?
ПСА после РПЭ считается нормальным, если находится в пределах 0,05—0,2 нг/мл. Повышенные показатели свидетельствуют о возможном рецидиве.
— Насколько можно доверять анализу крови на ПСА?
Существует несколько факторов, способных исказить результаты теста. При отсутствии злокачественных новообразований высокий уровень антигена может быть спровоцирован различными механическими воздействиями на простату, приемом некоторых лекарств, а также другими заболеваниями мочеполовой системы (простатитом, аденомой, инфекцией и пр.).
— ПСА-тесты выявили у меня рецидивирующий рак простаты. Врач предложил динамическое наблюдение. Значит ли это, что моя форма болезни неизлечима и терапия не имеет смысла?
Динамическое наблюдение — это не отказ от лечения, а одна из его разновидностей. Как правило, данную тактику предлагают больным, у которых карцинома растет медленно и едва ли когда-нибудь проявит себя. (Следовательно, она не обязательно должна повторно удаляться или облучаться ). Пациенту, находящемуся под динамическим наблюдением, необходимо регулярно обследоваться: врач отслеживает скорость роста раковых клеток, что позволяет ему своевременно обнаружить быстро прогрессирующую опухоль и перейти от выжидательной тактики к активному лечению.
— По результатам ПСА-анализа и биопсии мне диагностировали повторный рак простаты (T2bNxM0). Какие исследования еще нужно пройти, чтобы подтвердить диагноз?
В данном случае дополнительных исследований не требуется: на сегодняшний день биопсия простаты — это наиболее надежный метод подтвердить (или опровергнуть) онкологию.
Отслеживать норму пса после операции по удалению рака простаты необходимо регулярно — только так вы сможете уберечь себя от повторного развития болезни. Будьте здоровы!
Клиническая симптоматика заболевания определяется локализацией рецидивного новообразования и распространенностью онкологического процесса. На начальных стадиях рецидив рака простаты может протекать бессимптомно. При увеличении диаметра местной рецидивной неоплазии возникают симптомы, обусловленные механическим сдавлением мочеиспускательного канала, проходящего через предстательную железу или ложе удаленной простаты (в случае предшествующего оперативного вмешательства). Отмечаются частые позывы на мочеиспускание, прерывистое болезненное мочеиспускание, гематурия, никтурия, жжение во время и после мочеиспускания.
Наряду с перечисленными симптомами при рецидиве рака простаты могут наблюдаться расстройства половой сферы, в том числе – импотенция, эректильная дисфункция и гематоспермия. Возможны боли в паховой области. При проведении ректальной пальпации предстательной железы выявляется опухоль. При дальнейшем увеличении размеров местного рецидива отмечается прорастание шейки мочевого пузыря и прямой кишки. Возникают острая задержка мочи, запоры и примеси крови в каловых массах.
Проявления системного рецидива рака простаты определяются локализацией метастазов. Чаще всего страдает опорно-двигательный аппарат. При метастазах в кости (обычно в поясничный отдел позвоночника, реже в грудные позвонки, кости таза, бедренные кости и другие костные структуры) возникают боли в зоне поражения, при крупных очагах возможны патологические переломы. При поражении позвоночника наблюдаются неврологические расстройства. Наряду с вторичными очагами в костях при системном рецидиве рака простаты могут обнаруживаться метастазы в легкие, печень, почки и головной мозг.
Метастазы в легких проявляются болями в груди, кашлем и кровохарканьем. Поражение периферических отделов легких может протекать бессимптомно. Для рецидива рака простаты с метастазами в печень характерны боли, гепатомегалия и желтуха различной степени выраженности. Метастазирование в почки сопровождается болями в поясничной области, дизурией и гематурией. При метастатических опухолях мозга выявляются упорные головные боли, тошнота, рвота. Характер неврологических расстройств определяется локализацией метастатического рецидива рака простаты. На поздних стадиях наблюдаются истощение, гипертермия и симптомы раковой интоксикации.
Омельченко В.П.
Бова Ф.С.
Демидова А.А.
ФГБОУ ВО «Ростовский государственный медицинский университет» Минздрава РФ
ГБУ Ростовской области «Областная больница №2»
Цель. Повысить эффективность прогноза ранних рецидивов у больных с локализованным раком предстательной железы (РПЖ) после радикального хирургического лечения путем оценки экспрессии гена РСА3 в осадке и экзосомах мочи.
Материалы и методы. Обследованы 148 больных локализованным РПЖ. Всем пациентам в сыворотке крови исходно и каждые 3 месяца после радикальной простатэктомии (РПЭ) в течение двух лет определяли содержание простатспецифического антигена (ПСА) путем иммуноферментного анализа. Пациентов делили на две подгруппы в зависимости от наличия или отсутствия биохимического рецидива (БР).
В осадке и экзосомах мочи у пациентов методом ПЦР в реальном времени определяли экспрессию гена РСА3 относительно референсного гена KLK3.
Результаты. Уровень экспрессии гена РСА3 в экзосомах мочи у больных при РПЖ и ПИН-2 был выше при последующем рецидивировании по сравнению с благоприятным течением заболевания. При снижении в осадке мочи Ct РСА3–KLK3 менее 1,86 включительно, БР у пациентов с РПЖ и ПИН-2 в перитуморальной зоне развивались чаще (83% против 45%, р=0,008).
Заключение. Прогностическая значимость оценки экспрессии гена РСА3 в осадке и экзосомах постмассажной мочи для определения риска БР после РПЭ у больных с локализованным РПЖ выше по сравнению с определением ПСА в сыворотке крови. При повышении экспрессии гена РСА3 в осадке и экзосомах постмассажной мочи у больных с локализованным РПЖ риск БР в течение двух лет после РПЭ возрастает.
рак предстательной железы
простатспецифический антиген 3
1. Состояние онкологической помощи населению России в 2016 году / ред. А.Д. Каприн, В.В. Старинский, Г.В. Петрова. – М.: МНИОИ им. П.А. Герцена, 2017. – 236 с.
4. Louie K.S., Seigneurin A., Cathcart P., Sasieni P. Do prostate cancer risk models improve the predictive accuracy of PSA screening? A meta-analysis // Ann Oncol., 2015, vol. 26, no. 5, pp. 848-864.
6. Valadi H., Ekstrom K., Bossios A. Exosome-mediated transfer of mRNAs and microRNAs is a novel mechanism of genetic exchange between cells // Nat Cell Biol., 2007, no. 9, pp. 654–659.
7. Молекулярный канцерогенез / ред. М.А. Красильников, И.Б. Зборовская. – М.: ООО ИД «АБВ-пресс», 2016. – 418 c.
Целью работы явилось повысить эффективность прогноза ранних рецидивов у больных с локализованным РПЖ после радикального хирургического лечения путем оценки экспрессии гена РСА3 в осадке и экзосомах мочи.
Материалы и методы исследования
Работа выполнена в Центре урологии, нефрологии и гемодиализа, в патологоанатомическом отделении ГБУ Ростовской области «Областная больница № 2» в 2015-2017 гг. Все пациенты дали информированное согласие на участие в исследовании.
Критерии включения больных в исследование: 1) локализованный РПЖ (Т1с-Т2с);
2) выполнение больным радикальной простатэктомии (РПЭ); 3) отсутствие отдаленных метастазов.
Гистологические исследования в операционных биоптатах проведены у 148 больных с локализованным РПЖ (T1c–T2cN0M0). Возраст больных общей клинической группы колебался от 54 до 79 лет, составив в среднем 65,6±2,5 года. Распределение больных в зависимости от клинической стадии РПЖ было следующим: сТ1с – 9/148 (6,1%), сТ2а – 20/148 (13,5%), сТ2 – 43/148 (29%), сТ2с – 76/148 (51,4%). Высокая степень гистопатологической дифференцировки (≤6 баллов по Глисону) встречалась у 9/148 (6,1%), умеренная (7 баллов по Глисону) – у 137/148 (92,6%) и низкая (8-10 баллов по Глисону) – у 2/148 (1,3%) больных.
У всех больных гистологический тип опухоли ПЖ был представлен аденокарциномой.
Всем пациентам в сыворотке крови исходно и каждые 3 месяца после РПЭ определяли содержание ПСА путем иммуноферментного анализа на фотометре «Multiscan-Р 2» ( ., Финляндия). Основанием для заключения о биохимическом рецидиве (БР) были: превышение концентрации ПСА в крови более 0,2 нг/мл в трех последовательных измерениях, проведенных с интервалом 2 и более недель.
При выполнении генетических исследований на первом этапе пробоподготовки первую порцию мочи пациентов в объеме 70 мл собирали в контейнер после массажа ПЖ путем трехкратного нажатия на каждую долю. Непосредственно после сбора для получения образца мочевого осадка 20 мл мочи центрифугировали в течение 15 минут при 3000 об/мин. Далее супернатант удаляли, а оставшийся осадок ресуспендировали и отбирали 1,5 мл в пробирку «эппендорф». Осадок мочи консервировали, добавляя 1 мл «Среды РНК» (ООО «ИнтерЛабСервис», Россия). При выделении экзосом 50 мл мочи из полученной постмассажной порции центрифугировали в течение 15 минут при 10 000 об/мин. Полученный супернатант центрифугировали в течение 3 часов при 100 000 об/мин. Осадок промывали добавлением 3 мл буферного раствора PBS (phosphatebuffered saline), осаждали кратковременным центрифугированием. Далее экзосомы ресуспендировали в буфере PBS в объеме 200 мкл.
Выделение тотальной РНК из мочи осуществляли сорбентным методом набором «АмплиПрайм РИБО-сорб» («НекстБио», Россия) по шаговой инструкции производителя. Образцы обрабатывали ДНКазой (6 ед. активности) для удаления примеси геномной ДНК в течение 40 мин при комнатной температуре в соответствующем буфере (реагенты Applied Biosystems, США).
При обратной транскрипции использовали набор « » ( , США). При получении кДНК на РНК-матрице использовали метод отжига случайных олигонуклеотидов при расходовании 40,0 мкл набора и пошаговых этапах по инструкции производителя.
Экспрессию гена РСА3 в осадке и экзосомах мочи определяли методом полимеразной цепной реакции в реальном времени (ПЦР-РВ). При этом сравнивали величины пороговых циклов Ct изучаемого и референсного гена. В качестве референсного гена рассматривали ген калликреина человека KLK3, для которого характерна простатспецифичная экспрессия. Реакционная смесь содержала 1,0 мкл образца кДНК из осадка мочи или экзосом мочи, 8,0 мкл деионизированной воды, 1,0 мкл готовой смеси праймеров и TaqMan-зонда, 10,0 мкл концентрированного буферного раствора с полимеразой согласно протоколу производителя. Температурные параметры: начальная денатурация 95 °С в течение 10 мин, затем 47 циклов при 95 °С в течение 15 с, 60 °С – 1 мин (детекция).
При ПЦР-РВ использовали готовые праймеры 3 ( 02576345_1, , ), 3 ( 01371939_1, , ), а также TaqMan-зонды с красителями и малобороздочные лиганды MGB (minor groove binders, MGB). Образец мочи исследовали, если экспрессию KLK3 обнаруживали при значении порогового цикла Ct до 45 циклов. В каждом образце ген амплифицировали трехкратно и рассчитывали усредненное значение порогового цикла Ct.
Для проведения ПЦР реального времени использовали термоциклер Bio-Rad CFX96 (Bio-Rad, США), специализированное программное обеспечение — (. 2.1). Для выражения экспрессии гена РСА3 вычисляли показатель ΔСt = Сt(РСА3) – Сt(KLK3).
Статистическую обработку результатов проводили при использовании программы 12 (, США), модуля описательной статистики, частотного анализа, таблиц кросстабуляции. Рассчитывали медиану, 25 и 75 процентили. Различия количественных показателей между группами оценивали с помощью критерия Манна-Уитни при уровне значимости p≤0,05. Различия долей оценивали с помощью критерия c2. В работе использовали -анализ.
Результаты исследования и их обсуждение
Ретроспективно с учетом двухгодичных сведений о рецидивировании заболевания были проанализированы дооперационные результаты генетических исследований с учетом развития БР (табл. 1).
Содержание простатспецифического антигена в сыворотке крови и экспрессия гена РСА3 в осадке и экзосомах мочи у больных основной группы и группы сравнения в зависимости от рецидивирования заболевания
Примечание: р* — доверительная вероятность различия между подгруппами с наличием и отсутствием БР.
У пациентов с РПЖ вне зависимости от развития БР медиана и межквартильный диапазон величины ПСА в сыворотке крови перед операцией практически не различались (р=0,19) (табл. 1).
Значения медианы и межквартильного диапазона D гена РСА3 по сравнению с референсным геном KLK3 в осадке мочи были близки в двух изучаемых подгруппах в зависимости от течения заболевания и статистически значимо не различались (р=0,75) (табл. 1). Отрицательное среднее значение D изучаемого гена по отношению к референсному гену свидетельствовало о более высоком уровне экспрессии первого гена по сравнению со вторым.
Между тем в экзосомах мочи у пациентов с неблагоприятным течением заболевания установлен более высокий уровень мРНК гена РСА3 по сравнению с подгруппой больных без рецидивирования (р=0,04). Медиана D РСА3–LK3 в экзосомах мочи при биохимическом рецидивировании составила исходно -2,37, а в группе с благоприятным течением болезни -0,95 (табл. 1). Меньшее значение D свидетельствовало о более высоком уровне мРНК анализируемого гена РСА3 по сравнению с референсным геном KLK3 в экзосомах мочи.
Повышенная экспрессия гена РСА3 в экзосомах мочи была сопряжена с развитием БР в последующем. Для более детального изучения сопряжения между указанными процессами был предпринят частотный анализ и метод кросстабуляции (табл. 2).
Число больных РПЖ с различным уровнем экспрессии гена РСА3 в осадке и экзосомах мочи с учетом наличия или отсутствия БР
Примечания: р* — доверительная вероятность по критерию c2 при множественном сравнении.
Для осадка мочи разделительный уровень порогового цикла Ct для выделения больных с высоким риском рецидивирования заболевания составил -0,51. То есть, если у пациентов с аденокарциномой ПЖ ΔСtРСА3–KLK3 в осадке мочи был ниже значения -0,51 включительно, то с диагностической чувствительностью 87% и диагностической специфичностью 85% можно говорить о высоком риске БР в ближайшие 24 месяца после РПЭ. Доля ложноотрицательных случаев составила 13%, а ложноположительных – 15%. Общая диагностическая эффективность оценки экспрессии гена РСА3 в осадке мочи для прогноза раннего БР после РПЭ соответствовала 85%. Площадь под -кривой составила 0,802±0,0004 (<0,0001), что свидетельствовало о высокой информативности метода.
Итак, в нашей работе было выявлено, что оценка экспрессии гена РСА3 в осадке и экзосомах мочи информативна, но с определенными ограничениями, для прогноза развития БР в ближайшие 2 года после РПЭ.
1. Прогностическая значимость оценки экспрессии гена РСА3 в осадке и экзосомах постмассажной мочи для определения риска БР после РПЭ у больных с локализованным РПЖ выше по сравнению с определением ПСА в сыворотке крови.
2. При повышении экспрессии гена РСА3 в осадке и экзосомах постмассажной мочи у больных с локализованным РПЖ риск БР в течение двух лет после РПЭ возрастает. Диагностическая эффективность оценки риска прогрессирования локализованного РПЖ по уровню экспрессии гена РСА3, определенному методом полимеразной цепной реакции в режиме реального времени в осадке мочи составляет 85%, а в экзосомах мочи 87%.
Методы «спасительной» терапии применяются при местном или биохимическом рецидиве рака предстательной железы после проведения его лечения по радикальным программам.
Биохимическим рецидивом после радикальной простатэктомии (РПЭ) считают два последовательных повышения уровня ПСА более 0,2 нг/мл (таблица 1). После лучевой терапии, согласно критериям ASTRO – это три последовательных повышения уровня ПСА (Int. J. Radiat. Oncol. Biol. Phys., 1997). В настоящее время большинство специалистов (Roach М., 2006) склоняются к мнению, что после лучевой терапии (ДЛТ, брахитерапия) биохимический рецидив – это рост уровня ПСА на 0,2 нг/мл и выше надира
(критерии RTOG-ASTRO). После малоинвазивных аблятивных технологий, к которым относят HIFU- терапию, радиочастотную абляцию (РЧА) и криоабляцию, считают
биохимическим рецидивом повышение уровня ПСА выше 1 нг/мл (Aus G., 2006).
Определение биохимического рецидива после фокальных методов лечения является предметом дискуссии. До настоящего времени единого мнения не существует.
После констатации биохимического рецидива, необходимо ответить на вопрос: «Является ли это прогрессирование местным либо системным?». Для подтверждения
характера рецидива необходимо использование всех современных средств визуализации: ТРУЗИ предстательной железы, магнитно-резонансную томографию предстательной железы и органов таза (МРТ), компьютерную томографию забрюшинного пространства и таза для визуализации увеличенных лимфоузлов,
позитронно — эмиссионной томографии (ПЭТ), остеосцинтиграфии и биопсии предстательной железы после лучевых методов или зоны уретровезикального анастомоза после РПЭ. После лучевых методов и аблятивных технологий биопсию целесообразно выполнять не ранее, чем через 18 месяцев после проведенного лечения.
В настоящее время разработаны определенные критерии, которые предположительно позволяют дифференцировать местное прогрессирование от генерализации процесса после РПЭ. К этим критериям относятся: время повышения ПСА, время удвоения ПСА, дифференцировка опухоли по шкале Глисона и ее патоморфологическая стадия.
Так, например, о местном рецидиве после РПЭ с большой степенью вероятности можно судить, если подъем уровня ПСА больше 0,2 нг/ мл наблюдается не ранее, чем через
три года после операции, время удвоения ПСА составляет более 11 месяцев, показатель Глисона – менее 6, а патоморфологическая стадия – меньше, чем Т3а (Heidenreich A., 2010). Местный рецидив после лучевой терапии можно предположить при выявлении злокачественных клеток в биоптатах предстательной железы через 18 месяцев и при отсутствии метастатического поражения по данным КТ, МРТ и остеосцинтиграфии (таблица 1).
Таблица 1. Местный рецидив после РПЭ
A. Heidenreich, M. Bolla, S. Joniau, M.D. Mason, V. Matveev, N. Mottet, H-P. Schmid, T.H. van der Kwast, T. Wiegel, F. Zattoni. Guidelines on Prostate Cancer
Спасительные методы лечения РПЖ
К вариантам «спасительного» лечения относят: дистанционную лучевую терапию, РПЭ, высокодозную брахитерапию, криоабляцию и HIFU-терапию.
Чаще всего при местном рецидиве после радикальной простатэктомии выполняют спасительную дистанционную лучевую терапию (64-66 Гр на ложе предстательной железы). Показано, что чем меньше исходный уровень ПСА после выполненной РПЭ, тем лучше результаты лечения. Например, если ПСА до дистанционной лучевой терапии не превышал 0,2 нг/мл, то 5-летняя безрецидивная выживаемость достигает 77%, тогда как у пациентов с уровнем ПСА 0,2-1,0 нг/мл, она составляет 34% и 0% соответственно.
Дистанционная лучевая терапия возможна и после HIFU-терапии.
По данным Ward J.F. (2005) после выполнения ДЛТ 45 пациентам, перенесшим HIFU, 5-летняя выживаемость без биохимического рецидива составила 64%.
Спасительную радикальную простатэктомию (СРПЭ) нередко выполняют после дистанционной лучевой терапии (Bianco F.J. Jr.,2005). Пятилетняя выживаемостьбез биохимического рецидива после спасительной РПЭ колеблетсяот 47 до 65%, десятилетняя выживаемость – 30-43%. Пятилетняя канцерспецифическая выживаемость составляет 90-93%, 10-летняя – 70-77%. Вероятность прогрессии заболевания зависит от уровня ПСА перед спасительной РПЭ: при уровне ПСА менее 4 нг/мл выживаемость без биохимического рецидива составляет 86%, тогда как при ПСА 4-10нг/мл и более 10 нг/мл, 55% и 37%, соответственно (Gotto G.T., 2010).
Технически выполнить РПЭ после лучевой терапии достаточно сложно, поэтому частота осложнений после нее существенно выше, нежели после первичной радикальной простатэктомии. К наиболее частым осложнениям (таблица 2) по данным Gotto G.T. (2010) после СРПЭ относят: стриктуру уретровезикального анастомоза (до 26%), повреждение прямой кишки (1-2%), недержание мочи (до 56%), острую задержку мочеиспускания (до 10%), инфекционные осложнения (2%).
Таблица 2. Осложнения после СРПЭ и РПЭ
Geoffrey T. Gotto, 2010
Спасительная РПЭ возможна и после HIFU-терапии. Lawrentschuk N. (2011) опубликовал результаты о выполнении спасительной РПЭ 15 пациентам. Средний период наблюдения в этом исследовании составил 16 месяцев, в течение которых у 14 мужчин уровень ПСА не превысил 0,2 нг/мл. Однако у одного пациента, которого наблюдали в течение 24 месяцев, был отмечен уровень ПСА выше 0,2 нг/мл, что потребовало выполнения адъювантной лучевой терапии.
Спасительная РПЭ возможна и в случае местного рецидива после криоабляции предстательной железы. В литературе есть сообщение о 6 пациентах, которым выполнялась спасительная РПЭ (Grampsas S.A., 1995). Авторы отмечают, что через
12 месяцев наблюдения все пациенты были живы и отсутствовала прогрессия заболевания по уровню ПСА (ПСА менее 0,2 нг/мл).
Спасительная высокодозная брахитерапия (СВБТ) может выполняться после дистанционной лучевой терапии и перманентной брахитерапии. К показаниям относят: необструктивный тип мочеиспускания; время удвоения ПСА более 6 месяцев; сумма баллов по Глисону менее или равна 6; уровень ПСА менее 10 нг/мл; время предполагаемой продолжительности жизни более 5 лет.
Пятилетняя выживаемость без биохимического рецидива после выполнения СВБТ пациентам, перенесшим ДЛТ составила 34-38%, а после перманентной брахитерапии – 54% (Grado G.L., 1999, Lee H.K., 2008, Burri R.J., 2010).
Осложнениями, наиболее часто встречающимися при данном виде лечения, являются: острая задержка мочеиспускания – 14%, гематурия – 4%, дизурия – 6%, повреждения прямой кишки – 4%, ректальные кровотечения – 2%. (Grado G.L., 1999, Lee H.K., 2008, Burri R.J., 2010).
Спасительная криоабляция после ДЛТ представляется «идеаль
ной» для пациентов с клинической стадией менее Т2с; показателем Глисона менее 7, ПСА менее 10 нг/ мл на момент выполнения ДЛТ. «Идеальный» объем предстательной железы для выполнения криоабляции: 20-30 см3. Пятилетняя выживаемость без биохимического рецидива составляет 59% (таблица3).
Таблица 3. Результаты криоабляции после ДЛТ (Mohamed Ismail, 2007)
Применение методики затруднено при объеме железы более 40 см3 и распространении опухоли на семенные пузырьки. Осложнения после спасительной криотерапии (таблица 4): недержание мочи; задержка мочеиспускания; свищи; боли в промежности (Babaian R.J., 2008). Если ранее пациент перенес ТУР ПЖ, то грозным осложнением может явиться некроз уретры.
Таблица 4. Осложнения криоабляции после ДЛТ (Richard J. Babaian, 2008)
Спасительная криоабляция также возможна и после РПЭ. Siddiqui S.A. (2007) описал 15 подобных случаев. Под биохимическим рецидивом авторы подразумевали повышение уровня ПСА более чем на 0,1 нг/мл от достигнутого уровня. Безрецидивная выживаемость через 20 месяцев в его группе из 6 пациентов составила 40%.
Спасительная HIFU-терапия: показания для этого метода такие же, как и для спасительной криоабляции предстательной железы. Однако необходимо отметить, что для спасительной HIFU обструктивный тип мочеиспускания является относительным противопоказанием, а ТУР в анамнезе противопоказанием не является.
Опубликовано большое число работ о применении HIFU-терапии при местном рецидиве после ранее проведенной дистанционной лучевой терапии (ДЛТ). В одном из исследований выживаемость без биохимического рецидива на протяжении 3,2 лет составила 41% (таблица 5). Среди осложнений HIFU- терапии после ДЛТ в раннем после-операционном периоде чаще всего наблюдают задержку мочеиспускания. Свищи встречаются в 0-16% случаев; недержание мочи – в 5% случаев, стриктура уретры и склероз шейки мочевого пузыря – от 10 до 15% случаев (Huang W.C., 2010).
Таблица 5. Результаты спасительной HIFU-терапии при местном рецидиве РПЖ после ДЛТ (Willam C. Huang, MD, 2010)
Спасительная HIFU возможна и после брахитерапии. У нас имеется собственный небольшой опыт лечения с использованием аппарата Sonablate- 500: трем пациентам со стадией T2а-bNxM0 выполнялся HIFU при местном рецидиве после брахитерапии. Средний уровень ПСА перед процедурой составил 4,5 нг/мл. Период наблюдения составил от трех до девяти месяцев. Средний уровень ПСА после лечения – 0,3 нг/мл. Наличие имплантов в предстательной железе не препятствовало выполнению HIFU-терапии.
Спасительная HIFU-терапия выполнима и после РПЭ (рисунок 1). В одной из последних статей (Murota- Kawano A., 2010), 4 пациентам этот вид лечения был предложен после РПЭ. Средний уровень ПСА до лечения составлял 4,3 нг/мл, объем очага поражения – 4,6 см3. Всем больным после двухлетнего наблюдения выполнена биопсия, в результате которой злокачественных клеток найдено не было. HIFU после РПЭ возможна в том случае, если опухоль визуализируется. В противном случае – выполнение HIFU затруднено.
Рисунок 1. Спасительная HIFU-терапия (HIFU) после РПЭ
Больной 66 лет. В 2002 г. в лечебном учреждении по месту жительства перенес РПЭ. Дооперационный уровень ПСА составил 8 нг/мл, показатель Глисона – 5 (2 + 3); стадия T2bNxMo. Через 6 лет отмечено повышение уровня ПСА до 1,96 нг/мл. По данным ТРУЗИ и МРТ выявлено наличие резидуальных семенных пузырьков и объемное образование до 2 см у их основания. Выполнена биопсия семенных пузырьков и указанного образования. Заключение: аденокарцинома предстательной железы, показатель Глисона 8. Больному был выполнен сеанс HIFU с предварительной катетеризацией мочеточников. Через 9 месяцев уровень ПСА составил 0,02 нг/мл. Отмечено уменьшение в размерах очага рецидива и семенных пузырьков на 60%. Если до HIFU пациент получал гормональную терапию, то после проведенного лечения она была отменена. Отмечены некоторые улучшения эректильной функции. Недержания мочи отмечено не было.
• При местном рецидиве после РПЭ наиболее широко применяют ДЛТ. Перспективы применения HIFU и криоабляции на данный момент активно изучаются.
• При местном рецидиве после ДЛТ в качестве альтернативы РПЭ возможно применение аблятивных технологий – HIFU и криоабляции. Требуется изучение ближайших и отдаленных результатов.
• При местном рецидиве после перманентной брахитерапии наиболее перспективным также представляется использование HIFU и криоабляции.
• При местном рецидиве после криотерапии технически возможна повторная процедура, а при отсутствии эффекта – выполнение СРПЭ или ДЛТ.
• При местном рецидиве после HIFU-терапии технически возможно выполнение еще одного сеанса абляции, СРПЭ.
• Обилие методов спасительной терапии и их комбинированное применение открывает большие перспективы лечения РПЖ. Однако, необходимо накопление опыта и изучение отдаленных результатов.
Ключевые слова: рак простаты, сальважные методы, использование аппарата Sonablate-500,биохимический рецидив, местный рецидив.
Keywords: prostate cancer, salvage therapy, use of the deviceSonablate-500, biochemical failure, local recurrence.
Системный рецидив после радикальной простатэктомии
О таком виде рецидива рака предстательной железы говорят, когда обнаружены метастазы в лимфоузлах и других органах: позвоночник, печень, головной мозг, лёгкие. Самочувствие больного ухудшают общая слабость, боли и нарушение функции поражённых метастазами органов.
Местный рецидив после простатэктомии
Когда повышение специфического антигена не замечено вовремя и не приняты меры, на месте удалённой предстательной железы вырастает новая опухоль. Метастазов ещё нет. Если образование не выходит за пределы своей капсулы и сумма баллов по Глисону меньше 7, прогноз лечения благоприятный. Прорастание опухоли за пределы капсулы ухудшает шансы на желательный исход. Когда распространение обширное, захватывает семенные пузырьки, врачи предполагают плохой прогноз. На этом этапе появляются боли внизу живота, проблемы с мочеиспусканием и потенцией.
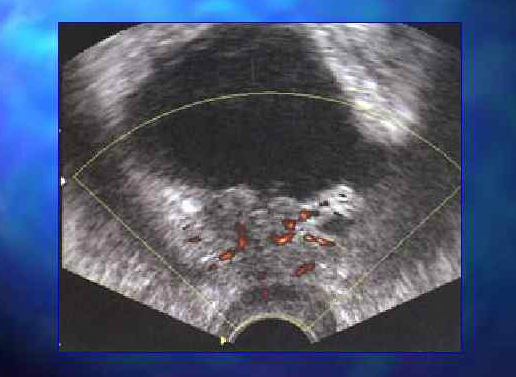
Диагностика и лечение рецидива рака простаты
Наряду с определением ПСА в процессе диагностики рецидива рака простаты используют данные объективного осмотра и ректального исследования, результаты КТ, МРТ и УЗИ органов малого таза, биопсию ложа предстательной железы и зоны анастомоза. Для выявления системного рецидива рака простаты с поражением опорно-двигательного аппарата выполняют сцинтиграфию костей скелета. При отсутствии клинической симптоматики и уровне ПСА ниже 20 нг/мл УЗИ и КТ обычно не показывают каких-либо патологических изменений. Более достоверные результаты удается получить при использовании эндоректальной МРТ.
При проведении биопсии образец, содержащий злокачественные клетки, удается получить у 54% пациентов. При наличии пальпируемого либо определяемого на УЗИ рецидива рака простаты эффективность биопсии увеличивается до 80%. Для обнаружения метастазов в печени проводят УЗИ, КТ или МРТ печени. При рецидивах рака простаты с метастатическим поражением почек выполняют урографию, при очагах в легких – рентгенографию органов грудной клетки. При метастазах в головном мозге проводят неврологический осмотр, осуществляют КТ и МРТ головного мозга.
Тактику лечения определяют с учетом локализации, диаметра неоплазии и распространенности рецидива рака простаты. Обычно применяют радиотерапию и гормонотерапию (самостоятельно либо в сочетании с облучением). Оперативные методики при рецидиве рака простаты используют редко. Хирургические вмешательства обычно выполняют при небольших локальных процессах у молодых пациентов. В качестве перспективного метода терапии местных рецидивов рассматривают ультразвуковую абляцию. При отсутствии эффекта после применения лучевой терапии и гормонотерапии пациентам с системными рецидивами рака простаты назначают химиотерапию.
Рецидив рака простаты — лечение в Москве
Результаты предыдущих исследований свидетельствуют, что примерно 30% мужчин с биохимическим рецидивом после хирургического лечения рака предстательной железы имеют клинический рецидив и только 16,4% умирают от данного заболевания.
Международная группа исследователей оценила, как биохимический рецидив рака предстательной железы ассоциирован с онкологическими исходами и какие клинические факторы определяют прогноз заболевания.
Рецидив рака простаты – повторное развитие злокачественной опухоли после радикального лечения рака предстательной железы. Может быть локальным, системным или биохимическим. Протекает бессимптомно либо проявляется болями, дизурией, гематурией, эректильной дисфункцией, гематоспермией и другими симптомами. При системном рецидиве рака простаты выявляются нарушения функций различных органов. На поздних стадиях отмечается выраженная общая онкологическая симптоматика. Диагноз выставляют с учетом анализа для определения уровня ПСА, МРТ, КТ, ПЭТ-КТ, сцинтиграфии и биопсии. Лечение – радиотерапия, гормонотерапия, операция, ультразвуковая абляция.
PSA после лечения онкологии
ПСА-тест — это в первую очередь инструмент, который позволяет контролировать эффективность назначенного врачом лечения. (Наиболее востребованные из современных методов — радикальная простатэктомия и лучевая терапия). Оценка адекватности обоих типов лечебного воздействия примерно одинакова, а динамика снижения уровня ПСА сильно разнится.
ПСА после простатэктомии
Радикальная простатэктомия (РПЭ) — операция, при которой пораженная опухолью простата и окружающие ее ткани полностью удаляются. В данном случае врачи рекомендуют сдавать ПСА-тест через 4—6 недель после оперативного вмешательства. Это обусловлено тем, что высокая концентрация простатоспецифического антигена сохраняется в крови еще какое-то время.
Уровень ПСА после радикальной простатэктомии находится в пределах нормы, если не превышает 0,2 нг/мл.
Когда результаты анализа пациента показывают большее количество онкомаркера, есть все основания подозревать биохимический рецидив рака предстательной железы.
Как часто нужно сдавать кровь на анализ?

ПСА после лучевого воздействия
Если обобщить отзывы пациентов, перенесших данный вид лечения, у подавляющего большинства из них уровень ПСА после лучевой терапии снизился примерно на 0,5 нг/мл (речь идет о результатах непосредственно после облучения!). Это связано с тем, что опухоль не уничтожается полностью, а «оставшиеся в живых» раковые клетки создают условия для дальнейшего роста антигенов.
Скорость снижения ПСА простаты после лучевой терапии зависит от митотического цикла опухолевых клеток: количество онкомаркера уменьшается постепенно (в среднем в течение двух лет). Если наблюдается его стабильное повышение, значит, карцинома по-прежнему существует, и требуются повторные терапевтические меры.
Резкий скачок ПСА после брахитерапии (контактная лучевая терапия) является нормой и не должен вызывать беспокойств.
Как часто нужно делать анализ?

Лечение рецидивов
Для уничтожения опухолевых клеток применяют:
На всех этапах проводят симптоматическую терапию для облегчения боли, улучшения самочувствия, устранения нарушений мочеиспускания.

Избежать рецидива рака предстательной железы после радикальной простатэктомии можно при чётком соблюдении рекомендаций уролога и контроле ПСА. Врачи Клиники урологии имени Р. М. Фронштейна помогут наладить онкологическое наблюдение и график обследований. Запишитесь на консультацию по телефону +7 (499) 409-12-45.
Акопян Гагик Нерсесович — врач уролог, онколог, д.м.н., врач высшей категории, профессор кафедры урологии ФГАОУ ВО Первый МГМУ им. И.М. Сеченова
Биохимический рецидив после радикальной простатэктомии
В течение первых пяти лет встречается у 15–42% пациентов. Физических симптомов рака простаты ещё нет. Человек чувствует себя хорошо, но внезапно появляется рост показателя ПСА выше 0,2 нг/мл по двум последним анализам крови. Врачи проводят дополнительное обследование, делают анализы крови и мочи, УЗИ, МРТ, при необходимости — остеосцинтиграфию и биопсию. По результатам выбирают способы лечения.
Лечение рецидива рака и PSA-тест
Если у пациента наблюдается рост уровня ПСА после простатэктомии или лучевой терапии, важно определить характер рецидива в зависимости от типа локализации.
В зависимости от методов первичной терапии, характера рецидива и индивидуальных особенностей пациента врач подбирает адекватное повторное лечение.





